胺
| 此条目需要扩充。 (2009年8月14日) |
胺(英语:amine)是氨分子(NH3)中的氢被烃基取代后形成的一类有机化合物。氨基(-NH2、-NHR、-NR2)是胺的官能团。
如果氮原子连着羰基(C=O),那么该化合物则称为酰胺,其化学性质与胺并不相同。
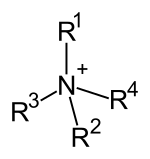
此外,胺还可根据氨分子上被取代的氢原子数量,顺次分为伯胺(一级胺)、仲胺(二级胺)、叔胺(三级胺)。此外,还有季铵盐(四级铵盐),可以看成是铵根离子(NH4+)的四个氢都被取代的产物。
| 一级胺 | 二级胺 | 三级胺 | 四级铵盐 |
|---|---|---|---|
| 伯胺 | 仲胺 | 叔胺 | 季铵盐 |
 |
 |
 |
|
一级胺及二级胺的物理性质主要受氢键影响,然而因为氮与氢阴电性的差别(3.0-2.1=0.9)并无氢和氧间(3.5-2.1=1.4)那么大,所以一般 N-H...H氢键较不像O-H...H键那么强,故胺的沸点一般较相对的磷烃为高,却低于相对应的醇。 例如,
| 乙烷 | 甲胺 | 甲醇 | |
|---|---|---|---|
| 分子量 | 30 | 31 | 32 |
| 沸点 | -88 | -7 | 65 |
甲胺和乙胺在室温之下为气体,但甲醇和乙醇在室温之下为液体。甲醇与甲胺分子量相近,其沸点差异却甚大。 几乎所有胺类皆与水形成氢键,所以比同分子量的烃易溶于水,低分子量的胺类与水完全互溶,高分子胺类只适量溶于水。 气体胺带有一种类似氨的气味,液体胺则带有一种容易辨出的鱼腥味。

|
⇌ | 
|
| 胺的手性翻转 | ||
氮原子连有三个不同基团形如NHRR′与NRR′R″的胺是有手性的,因氮有一对孤对电子,分子呈三角锥形,氮是手性中心。唯其手性翻转能垒相对很低,对于三烷基胺通常只需活化能25-37.6 kJ/mol,两个对映体在室温下就能迅速转化故对映体不能分离。[1]若季铵盐氮所连四个基团不同,则能拆分出旋光异构体。有些环状的胺因位阻不能翻转成对映体也能拆分。
氨或胺氮上有孤对电子,作为亲核试剂与卤代烷发生亲核取代反应,按SN2机理进行。许多有机卤化物以氨水溶液或氨溶液处理则变成胺类:
- RX + NH3 → RNH3 + X-
- RNH3+X- + NH3 → RNH2 + NH4+ + X-
- (X为卤素)
胺的主要合成方法是氨的烷基化。工业上使用醇与氨合成有机胺:
- ROH + NH3 → RNH2 + H2O
这些反应需要使用催化剂、特制仪器及额外纯化,因为得到的是一、二、三级胺的混合物,需要提高反应的选择性。
其它胺合成方法见下表:
| 反应名称 | 原料 | 注释 |
|---|---|---|
| 盖布瑞尔伯胺合成反应 | 卤代烷 | 试剂:邻苯二甲酰亚胺。制备一级胺的高选择性方法。 |
| 施陶丁格反应 | 叠氮化物 | 也可使用还原剂四氢铝锂。 |
| 施密特反应 | 羧酸 | |
| Template:En-link | 亚胺 | 烯丙基胺的合成 |
| 霍夫曼降解 | 酰胺 | 只适用于制备一级胺,并且不会有二三级胺副产物。 |
| 霍夫曼消除反应 | 季铵盐 | 强碱处理得季铵碱,再消除 |
| 酰胺还原 | 酰胺 | 酰胺被强还原剂如四氢铝锂还原 |
| 腈催化加氢 | 腈 | |
| 硝基化合物的还原 | 硝基化合物 | 还原剂可以是锌,锡,铁,在酸溶液中 |
| 德尔宾反应 | 卤代烃 | 试剂六亚甲基四胺 |
| Buchwald–Hartwig偶联反应 | 卤代芳香烃 | 合成芳胺的重要方法。 |
| 门秀金反应 | 叔胺 | 生成季铵盐 |
| 胺加成 | 烯烃与炔烃 | |
| Hofmann–Löffler–Freytag反应 | N-卤代胺 |
- ↑ 邢其毅等.《基础有机化学》第三版 下册.北京:高等教育出版社,2005年.ISBN 978-7-04-017755-8
